Пациент И., 52 года, поступил в стационар Тюменского областного кожно-венерологического диспансера с жалобами на интенсивный кожный зуд, покраснение, выраженную сухость кожи, расчесы, отек кожи в области сгибов крупных суставов с трещинами и обильным шелушением кожи туловища.
Из анамнеза известно, что первые симптомы поражения кожи появились в детском возрасте, диагноз нейродермит установлен сразу, протекал с обострениями 3 и более раз в год, в весенне-летний период.
В последствии диагноз был изменен на атопический дерматит, проводилось лечение топическими ГКС, ингибиторами кальциневрина, антигистаминными препаратами, увлажняющими и смягчающими средствами. В последние 3 года заболевание рецидивирует чаще 4-х раз в год, сопровождается сильным зудом и вторичным инфицированием. Неоднократно получал лечение в стационаре ОКВД, в том числе преднизолон до 60 мг в/в и антибактериальная терапии инфекционных осложнений экскориаций. Эффект от терапии был удовлетворительный.
При поступлении состояние средней тяжести. Конституция гиперстеническая. Аллергологический анамнез и наследственность не отягощены. Живот мягкий, безболезненный при пальпации. Печень, селезенка не увеличены. Стул регулярный, без патологических примесей. Симптом поколачивания отрицательный с обеих сторон. Мочеиспускание безболезненное. Щитовидная железа визуально не увеличена, пальпация ее безболезненная. Лимфатические узлы пальпируются по задней поверхности шеи и в подмышечных областях, безболезненные, подвижные, мягкоэластичной консистенции. Носовое дыхание не затруднено. Над всей поверхности легких ясный легочный перкуторный звук. Дыхание везикулярное, хрипы не прослушиваются. ЧДД 18 в минуту. Тоны сердца ясные, ритмичные, ЧСС 74 в минуту, артериальное давление 130/80 мм рт. ст. Язык влажный, розовый. ЭКГ: ритм синусовый, ЧСС 78 в минуту. КТ-признаков очаговых и инфильтративных изменений в паренхиме легких не выявлено. УЗИ органов брюшной полости, забрюшинного пространства, щитовидной железы и паращитовидных желез патологии не выявило.
Патологический процесс носит распространенный характер. Представлен разлитой эритемой кожи туловища, конечностей, трещины в локтевых и подколенных сгибах, обильное лихеноидное шелушение с линейными следами расчесов по всей поверхности кожи без признаков пиодермии. В области розовой каймы губ проявления хейлита. Ногти на руках имеют полированный блеск. Индекс SCORAD – 84.
Лабораторные и инструментальные исследования при поступлении. Клинические анализы крови и мочи в пределах нормы. Показатели биохимического анализа крови в пределах нормы. Гормоны щитовидной железы в пределах нормы. Иммуноглобулины А, М, G в сыворотке крови в пределах нормы. Уровень СРБ в крови – 8 мг/л. Общий IgЕ более 1000 МЕ/мл. Обследование на гельминтозы не выявило контаминации.
На основании жалоб, анамнеза заболевания, клинической картины и результатов обследования поставлен диагноз: атопический дерматит, распространенная форма, тяжелое течение, фаза выраженных клинических проявлений, осложненный травматическими экскориациями.
В стационаре проводилось лечение: метилпреднизолон 250 мг внутривенно в 200 мл физиологического раствора 7 дней, лоратадин 10 мг внутрь 7 дней, топическая терапия мометазоном. Эффект от проводимого лечения незначительный – зуд уменьшился, снизилась инфильтрация кожи в области локтевых сгибов и подколенных областей, но обилие экскориаций и трещин с мокнутием сохраняется.
Это стало обоснованием для прецизионной диагностики путем оценки цитоиммунограммы кожи (табл. 3.16).
Таблица 3.16. Цитоиммунограмма кожи больного И., 52 года, от 28 июня 2015 года № 89/1

Поскольку было обнаружен репаративный потенциал эндотелиальных клеток (их присутствие, но без должной активности к репарации), что подтверждается значениями CD146+ и CD146+CD34+ соответственно, с целью профилактики вторичного инфицирования эрозивных поражений кожи и скорейшей эпителизации, к общей топической терапии мометазоном было добавлено биотехнологическое средство Cellgel на эрозивные поражения кожи и трещины 2 раза в день, 10 дней.
Была отмечена положительная динамика кожного процесса: на фоне общего уменьшения площади поражения кожи и значительного снижения выраженности лихенификации кожи, отмечен регресс вторичных элементов (эрозии и чешуе-корки). Нежелательных эффектов отмечено не было. По мнению больного, такого «комфортного состояния кожи» он не отмечал более 10 лет (рис. 3.49).

Рисунок 3.49. Клиническая демонстрация эффективности топической терапии эрозивных поражений кожи у больного И., 52 года, от 28 июня 2015 года № 89/1 и 9 июля 2015 года № 89/2
Одновременно с клинической эффективностью, проявленной снижением индекса SCORAD с 84 баллов до 22, было обнаружено снижение количества клеток в пробе, отвечающих за развитие воспалительного процесса и увеличение количества активированных эндотелиальных клеток в очаге воспаления – CD146+CD34+ – 0,2% до лечения и 8,9% после (табл. 3.17).
Таблица 3.17. Цитоиммунограмма кожи больного И., 52 года, от 9 июля 2015 года № 89/2
Эффект от применения биотехнологического средства делает перспективным дальнейшее его применение у пациентов с тяжелым течением атопического дерматита, сопровождающегося эрозивными осложнениями и экскориациями и позволяет предложить концепцию прецизионной диагностики и применения биотехнологического средства Cellgel в топической терапии атопического дерматита (рис. 3.50).

Рисунок 3.50. Концепция прецизионной диагностики и применения биотехнологического средства Cellgel в топической терапии атопического дерматита
Таким образом, было установлено, что между составляющими компонентами разработанного биотехнологического средства Cellgel и данных прецизионной диагностики воспалительного инфильтрата у больного атопическим дерматитом, существует тесная иммунопатогенетическая связь, что обеспечивает репаративное действие и обуславливает высокую эффективность средства в качестве дополнения к топической терапии. Назначение разработанного биотехнологического средства выглядит обоснованным для топической терапии больных, страдающих тяжелыми формами атопического дерматита, клинические проявления у которых сопровождаются эрозивными поражениями и трещинами кожи.
С целью оптимизации топической терапии, проведено экспериментальное определение наличия или отсутствия репаративного действия разработанного биотехнологического средства на эрозивно-язвенные поражения кожи больных вульгарной пузырчаткой. Для этого, автором был получен патент РФ на изобретение № 2481115 от 23.03.2012.
Больная Я., 55 лет, обратилась в Тюменский областной кожно-венерологический диспансер в декабре 2018 г. с жалобами на распространенные симметричные высыпания на коже туловища и конечностей. Со слов больной, заболела остро, летом этого года. После появления первых признаков заболевания – единичных красных пятен на туловище, сопровождавшихся умеренным зудом, обратилась к дерматологу по месту жительства. Был поставлен диагноз «Дерматит?» и назначена симптоматическая терапия комбинированным ГКС. Спустя несколько дней, на фоне пятен стали появляться пузырьки. При обращении в ОКВД была госпитализирована для уточнения диагноза.
История жизни, наследственный и аллергоанамнез без особенностей.
При поступлении, патологический процесс носил распространенный характер, локализуясь на коже туловища, верхних и нижних конечностей, был представлен множественными округлыми, местами отечными эритематозно-сквамозными очагами розового и светло-розового цвета и пятнами гиперпигментации коричневого цвета. На поверхности отдельных очагов поражения, преимущественно в области груди, спины, поясничной области, имелись сгруппированные пузырьки с серозным содержимым на гиперемированном фоне. На коже боковых поверхностей туловища, ягодиц и верхней трети плеч определялись овальные и круглые, сливающиеся между собой эрозии до 1 см в диаметре с корочками и чешуйками на поверхности пораженных участков кожи. Феномен Никольского был положительным. Придатки кожи и слизистые оболочки в процесс не были вовлечены.
Клинический диагноз при поступлении: Пузырчатка обыкновенная? Пузырчатка листовидная? Герпетиформный дерматит Дюринга?
Учитывая тяжелое состояние, стремительность развития пузырьковых и эрозивных элементов, возраст больной и положительный симптом Никольского была проведена диагностическая биопсия с кожи спины с гистологическим исследованием.
По результатам гистологического исследования были выявлены изменения, которые потребовали дополнительных диагностических мероприятий. А именно: «эпидермис неравномерен с выраженным гиперкератозом и спонгиозом, клетки зернистого слоя разобщены между собой с тенденцией к образованию пузыря, в сосочковом слое дермы отёк и диффузная лимфоцитарная инфильтрация с эозинофилами». Для уточнения диагноза было рекомендовано проведение РИФ и получение цитоиммунограммы (автором оформлен Патент РФ № 2630607 от 02.06.2016).
По результатам комплексного клинико-лабораторного обследования выявлено положительный мазок-отпечаток на акантолитические клетки, лейкоцитоз (12,8*109/л) периферической крови, лимфопения (1,9 тыс/мкл), повышен уровень АЛТ составил 72 Ед/л, по результатам проведения нРИФ с антителами к IgG, IgA, IgM в биоптате видимо непоражен- ной кожи наблюдалась умеренная фиксация IgG в межклеточных промежутках эпидермиса с понижением градиента фиксации от зернистого и рогового слоев к базальному.
Дополнительные сведения, полученные от прецизионной диагностики путем оценки цитоиммунограммы кожи (табл. 3.18), показали наличие репаративного потенциала в очагах воспаления.
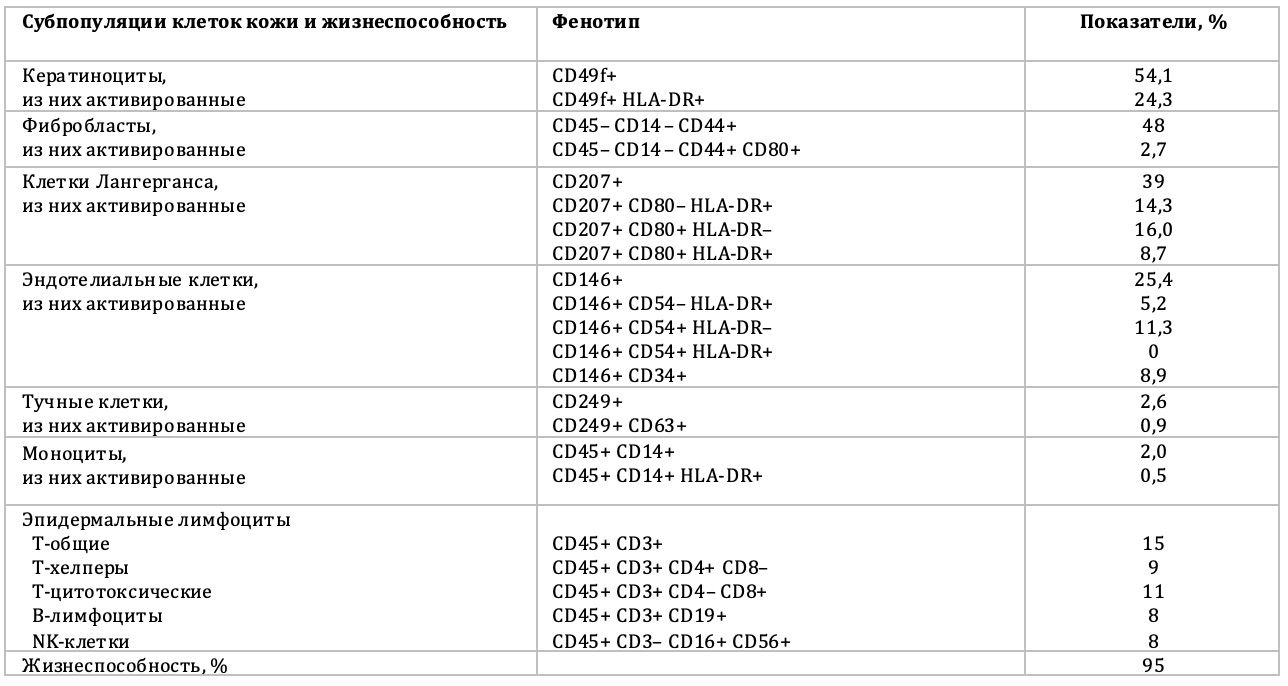
Таблица 3.18. Цитоиммунограмма кожи больной Я., 55 лет, от 12 декабря 2017 года № 111/2

В условиях стационара больной было проведено следующее лечение: таблетированный преднизолон из расчета 1 мг на кг массы тела в дозе 90 мг в сутки 30 дней, эссенциальные фосфолипиды по 5 мл в/в струйно, №5, «Панангин» по 1 табл. 3 раза 30 дней, «Кальций Д3» по 1 табл. 3 раза в сутки, наружная терапия мометазона фуроатом и раствором метиленового синего.
С целью скорейшей эпителизации эрозий и учитывая сведения цитоиммунограмм о наличии репаративного потенциала клеток кожи с фенотипом CD146+CD34+ – 1,1%, было рекомендовано применение биотехнологического средства Cellgel на эрозивные поражения кожи 2 раза в день, 30 дней.
На фоне терапии отмечалась выраженная положительная динамика в виде регресса большинства высыпаний с формированием пятен гиперпигментации. По результатам проведенного лечения больная была выписана с улучшением под наблюдение врача-дерматовенеролога по месту жительства в амбулаторных условиях и последующим решением вопроса о дальнейшем снижении суточной дозы принимаемого ГКС (рис. 3.51).
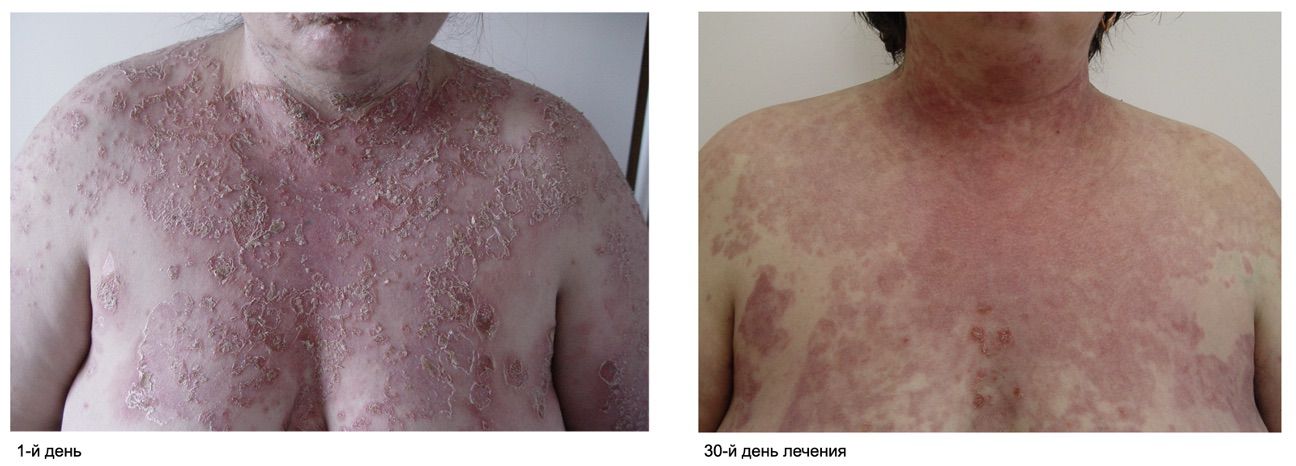
Рисунок 3.51. Клиническая демонстрация эффективности топической терапии эрозивных поражений кожи у больной Я., 55 лет, от 12 декабря 2017 года и 11 января 2018 года
По результатам последующего наблюдения, отмечалась стойкая клиническая ремиссия заболевания – новые высыпания не появлялись. Спустя два месяц после стационарного лечения суточная доза системного глюкокортикостероида была уменьшена с 60 мг в сутки на момент выписки, до 45 мг в сутки.
Было установлено, что между составляющими компонентами разработанного биотехнологического средства существует тесная иммунопатогенетическая связь, что обеспечивает сочетанное, синергичное пролиферативное и аниапоптотическое действие и обуславливает высокую эффективность средства в лечебном плане. Эта связь может быть отражена в концепции прецизионной диагностики и применения биотехнологического средства Cellgel в топической терапии вульгарной пузырчатки (рис. 3.52.).
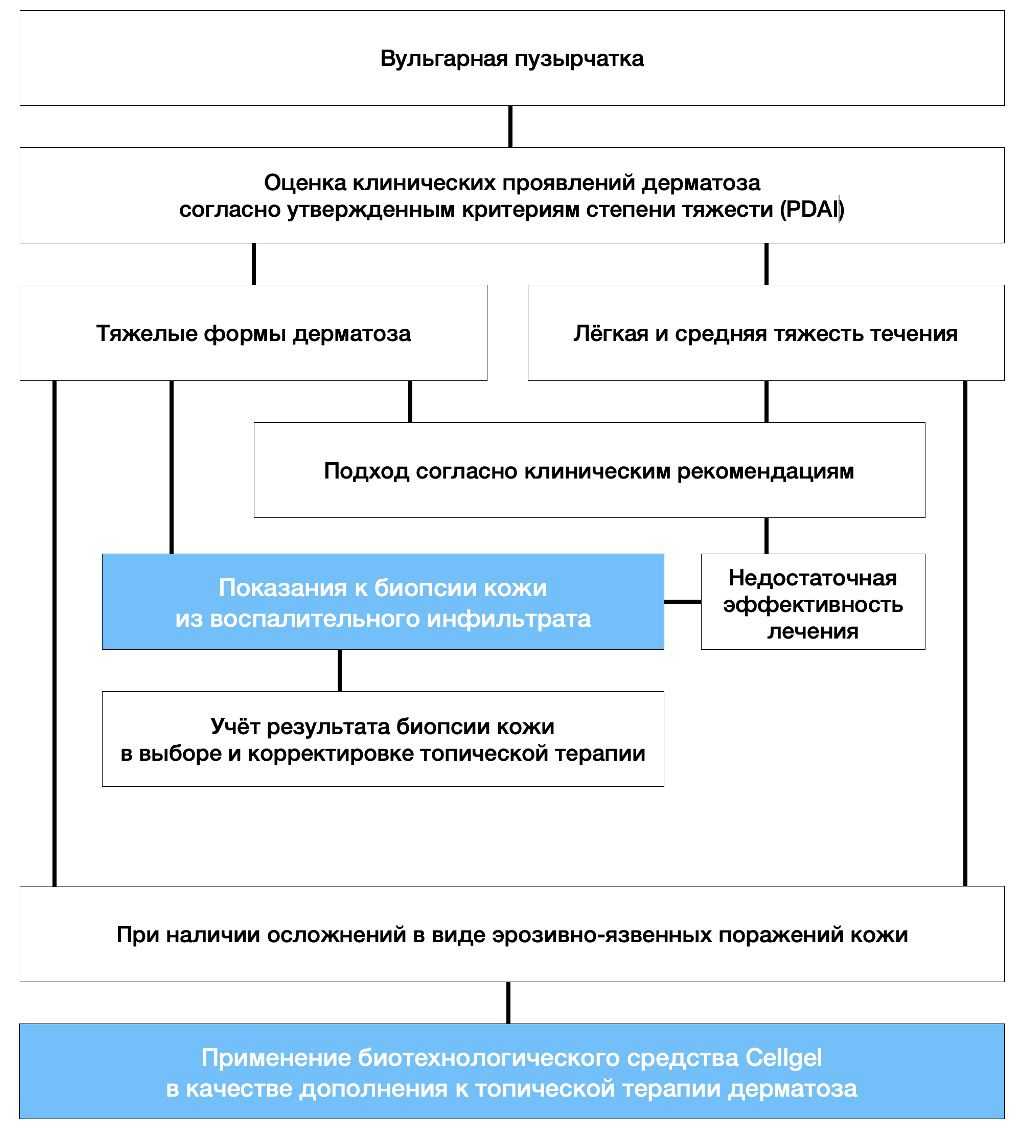
Рисунок 3.52. Концепция прецизионной диагностики и применения биотехнологического средства Cellgel в топической терапии вульгарной пузырчатки
Таким образом, назначение разработанного биотехнологического средства Cellgel выглядит обоснованным для топической терапии больных, страдающих вульгарной пузырчаткой.