Современная медицинская наука, благодаря техническому перевооружению, подошла к изучению сложных, многосвязных и неопределенных процессов. Детерминистский (причинно-следственный) и стохастический (многократно-повторяемый) подходы, при которых на протяжении многих лет выявлялись значимые симптомы и их совокупности, определялись средние величины и, на этом основании, стандартизировались подходы к диагностике и лечению, оказываются малополезными [255].
Тенденции развития дерматологии наглядно демонстрируют, что ее достижения связаны не только с наблюдениями, но и новыми технологиями исследовательской деятельности. Приняв тот факт, что кожа человека представляет собой активный орган иммунной системы, а резидентные и рециркулирующие клетки эпидермиса и дермы способны не только инициировать иммунные процессы, но и определять состояние кожных покровов, была обозначена актуальность изучения кожи путем определения фенотипа её клеток.
Однако, полифункциональность сложность кожи, с многообразием субпопуляций клеток и их отношений, а главное – их спаянность в структурный конгломерат, не позволяли избирательно осуществлять изучение. Подход к преодолению этого практического затруднения открылся в ходе ряда исследований свойств и функциональных состояний субпопуляций клеток кожи, выполненных автором в 2012–2020 годы.
По результатам нескольких патентованных изобретений исследовалась динамика состояний субпопуляций клеток кожи человека. Сама возможность этих исследований возникла после изобретения способа разделения клеток кожи при сохранении их жизнеспособности. Автором были оформлены Патент на изобретение «Способ получения жизнеспособной гетерогенной популяции клеток кожи» (Приложение 1) и Патент на изобретение «Способ определения субпопуляционного состава клеток кожи и получения цитоиммунограммы кожи» (Приложение 2), что нашло отражение в Резолюции Х Международной конференцией иммунологов Урала (Тюмень, 2012). Использование в данной работе изобретенных способов, позволило продемонстрировать возможности определения среднестатистических значений параметров фенотипического статуса клеток кожи условно здоровых лиц.
Открывшиеся при этом иммунологические феномены состояний кожи позволили предложить новый подход в прецизионной диагностике иммуноопосредованных дерматозов. Цитоиммунограмма кожи, оформляемая по факту применения разработанных способов, проста в исполнении и доступна, позволяет фиксировать информацию о количественном составе и функциональной активности клеток кожи, что объективно свидетельствует о текущем статусе локального компартмента иммунитета пациента.
Для этого, в качестве базового набора маркеров дифференцирующих субпопуляции клеток и характеризующих динамику мембранных событий этих субпопуляций, были впервые предложены: CD3, CD4, CD8, CD14, CD16, CD19, CD34, CD44, CD45, CD49, CD54, CD63, CD80, CD146, CD203c; CD207, CD249. Практическое значение данного решения заключается в возможности определения начального фенотипа клеток в воспалительном инфильтрате кожи, позволяет провести многопараметрический анализ клеток кожи в биоптате кожи пациента. Начало этой, более точной – прецизионной диагностике положено, но уже сейчас оно закладывает основание для будущих практических реализаций, поскольку впервые дерматология приблизилась к возможности разрешения противоречия между наблюдаемыми симптомами и скрытым множеством феноменов на уровне клеток кожи.
Дополнительно показанная в работе возможность исследовать криоконсервированный образец биоптата кожи позволяет сделать повторное исследование спустя некоторое время или после каких-либо процедур, воздействий, применении наружных средств. Широкомасштабное применение цитоиммунограммы в перспективе позволит создать половозрастной регистр состояния кожи в норме и патологии, что позволит определять степень реагирования кожи на воздействия среды, измерять активность субпопуляций клеток кожи в условиях нормы и патологии, использовать критерии возрастных изменений кожи, объективно оценивать динамику заболевания кожи, индивидуально подбирать и контролировать эффективность применения наружных лекарственных средств.
Выражаемые маркерами функциональной активности, количественные изменения молекул на поверхности клеток отражают истинность мембранных событий, которые приводят к качественным изменениям кожи в виде появления разнообразия элементов сыпи. Понимание этой связи позволит сформировать фронт решений актуальных проблем дерматологии. Так, длительное время остаётся актуальным спрос на научные разработки, ускоряющие ранозаживление кожи.
Возможность отследить динамику поведения молекул и клеток позволила подойти к решению проблемы строго, учитывая хаотическую природу изучаемого объекта. Став первой инвазивной методикой, оценивающей не только структурное состояние клеток кожи, но и определяющей функцию её субпопуляций, цитоиммунограмма кожи помогла выявить объект целенаправленного воздействия в патогенезе раневого процесса. Гипотеза о возможной стимуляции репаративных потенций в коже путем внесения вещества ксеногенного происхождения, предсказуемо воздействующего на механизм формирования грануляционной ткани, которая как известно является обязательным этапом к последующей эпителизации и формированию эстетического результата, реализовалась с возможностью применения цитоиммунограммы кожи в исследовании клеток фенотипа CD34+CD45dim. Последние оказались основополагающими в осуществлении эпителизации посредством их активации веществом ксеногенного происхождения.
Действующим веществом был предложен супернатант клеток фенотипа CD34+CD45dim куриного SPF-эмбриона в гелеобразующем биополимере на основе гидроксиэтилцеллюлозы.
В ходе дальнейших исследований были получены данные о дозозависимом влиянии концентрации действующего вещества на жизнеспособность и процессы апоптоза клеток в культуре. Этот результат позволил спланировать и провести исследование в условиях экспериментального заживления ран с участием лабораторных животных.
Экспериментальным путем было установлено, что для получения отчетливого эффекта в суспензии должна содержаться определенная концентрация клеток фенотипа CD34+CD45dim. При попытке уменьшения концентрации клеток фенотипа CD34+CD45dim значительно снижался репарационный эффект. В свою очередь повышение концентрации выше разработанного уровня не приводило к существенному увеличению эффективности средства. Кроме того, вступая во взаимодействие с рецепторным полем раны, обладая при этом широким спектром противомикробного действия, проявляя активность в отношении грамположительных и грамотрицательных бактерий, грибов рода Candida и дерматофитов, вещество прогнозировано стимулировало миграцию и пролиферацию фибробластов, кератиноцитов, эндотелиальных и других клеток, активно участвующих в ранозаживлении. Действуя как катализатор грануляционного роста, вещество безопасно, стерильно, не токсично, запускает процессы пролиферации и обладает бактериостатической активностью, способствуя эпителизации, восстановлению эластичности тканей, нормализации ориентации и вызревания коллагеновых волокон, предупреждая патологическое рубцевание.
Это стало основанием для оформления Патента на изобретение «Средства для заживления ран «Cellgel», способ его получения и способ лечения ран различной этиологии полученным средством» (Приложение 3), в основе которого использован эффект активации клеток с фенотипом CD34+CD45dim кожи посредством избирательного воздействия молекул адгезии. Контрактный выпуск разработанного биотехнологического средства был организован в Федеральном государственном автономном научном учреждении «Федеральный научный центр исследований и разработки иммунобиологических препаратов им. М.П. Чумакова РАН», а применение разрешено Протоколом лабораторных испытаний № 374 КХ Федерального агентства по техническому регулированию и метрологии ФБУ «Государственный региональный центр стандартизации, метрологии и испытаний в Москве и московской области» от 21.06.2021 (Приложение 9), Протоколом лабораторных испытаний № 62Л/З-31.01/23 от 31.01.2023 (Приложение 10) и Протоколом испытаний № 594-12П/7-НТ от 24.12.2012 и декларациями Таможенного Союза о соответствии № ТС RU Д-RU.АЛ14.В.03012 от 25.12.2012 г. и № ЕАЭС RU Д-RU.РА01.В.56185/21 от 25.06.2021 (Приложение 12).
Разработанное с учетом целевого воздействия, новое биотехнологическое средство продемонстрировало высокую эффективность ранозаживления при повреждениях кожи различной этиологии. Производство ранозаживляющего средства Cellgel стало инновационным, а экономичность оправданной, что позволило стать лауреатом Всероссийского конкурса Программы «100 лучших товаров России», а применение стало основой дальнейших клинических наблюдений.
Было установлено, что между компонентами разработанного биотехнологического средства и данными прецизионной диагностики воспалительного инфильтрата у больного атопическим дерматитом и вульгарной пузырчаткой, клинические проявления у которых сопровождаются эрозивными и эрозивно-язвенными поражениями кожи, существует тесная иммунопатогенетическая связь. Это обеспечило сочетанное, пролиферативное, аниапоптотическое, репаративное действие и обусловило высокую эффективность средства в качестве дополнения к топической терапии при данных заболеваниях кожи.
Дальнейшее назначение для постпроцедурного ухода за поврежденной кожей также показало высокую эстетическую и симптоматическую эффективность, что обосновывает его применение в косметологии и пластической хирургии.
Вышесказанное было отражено в сводной концепции прецизионной диагностики и применения биотехнологического средства Cellgel в топической терапии иммуноопосредованных дерматозов (рис. 3.79).
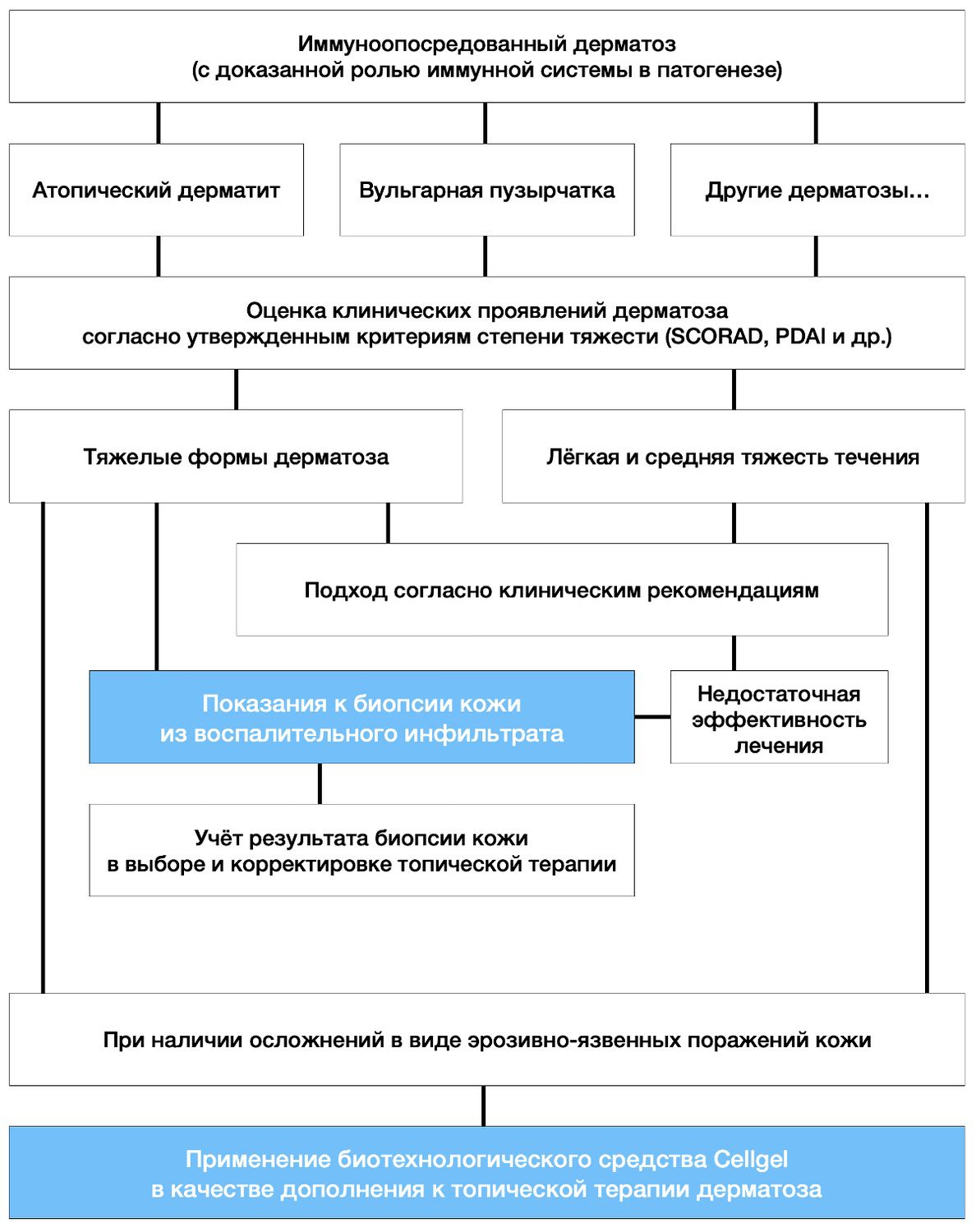
Рисунок 3.79. Концепция прецизионной диагностики и применения биотехнологического средства Cellgel в топической терапии иммуноопосредованных дерматозов
Описание результатов проведенных наблюдений вызвало необходимость выхода к мобилизации методов концептуального анализа для различения фенотипов субпопуляций клеток кожи. Это решение обнаружило классы потенциальных ситуаций, которые до сих пор не были различимы в дерматологии. В данной области исследовательской практики существенным оказалось то, что можно назвать дефицитом концептов для объяснения наблюдаемых феноменов.
Решение этой части научной проблемы было задумано вести на основе инструментария научно-технического направления, основанного российским ученым в области методологии разработки информационных систем С.П. Никаноровым, и созданных им технологий концептуального анализа. Они направлены на конструирование понятий в тех областях практики, которые нуждаются в строгих различениях реальности [239]. Применение концептуального анализа ориентировано на получение практически значимых результатов [175], позволило теоретически развить итоги исследований клеток кожи человека до внедрений в практику и достоверного прогноза. На основе типологизации концептуального разнообразия признаков клеток кожи, были построены три концепта: «Множество всех подмножеств признаков клетки», «Множество видов клеток и множество их функций», «Множество подмножеств видовых клеток вместе с множеством подмножеств их функций», где каждая субпопуляция, состоящая из клеток одновременно всех видов, отражает специфическую функционально-клеточную структуру элементарного фрагмента кожи и представляет собой ее специфический фенотип.
Это позволило выйти на широкий класс исследовательских задач в дерматологии, опирающейся на различия фенотипов субпопуляций клеток кожи, а переход от симптоматического подхода в лечении заболеваний кожи к фенотипическому является переходом к дерматологии нового типа – фенотипической дерматологии. В ее основание должны быть положены сведения о свойствах всех возможных фенотипов субпопуляций клеток кожи. За каждым типом таких задач стоит проблема распознавания частных свойств сложной морфологии клеток кожи:
Это задачи, которые не могли быть поставлены прежде.
В качестве примера было показано практическое решение только одной из перечисленных задач, а именно – выявление способа целенаправленного изменения переходов между состояниями субпопуляций клеток. Конкретно, путём разработки технического устройства для избирательной активации in vitro клеток кожи определенного фенотипа.
Практическая ценность решения данной задачи определена постановлением Правительства Российской Федерации и приказом Минэкономразвития об обеспечении государственного контроля качества исследований парфюмерно-косметической продукции для осуществления процедуры оценки соответствия требованиям технического регламента Таможенного союза «О безопасности парфюмерно-косметической продукции» ТР ТС 009/2011 (Федеральный закон от 28.12.2013 № 412-ФЗ ред. от 23.06.2014 «Об аккредитации в национальной системе аккредитации»).
В ходе выполнения работы, данная задача была решена изобретением и регистрацией Патента на полезную модель «Устройство для активации репаративных потенций клеток кожи» (Приложение 4). С одной стороны, это устройство – отклик на потребность внедрения в практику дерматологии экспертных систем. С другой стороны – оно открывает возможность для создания ряда решений по так называемой «адресной доставке» активных веществ. Практическое назначение изобретения было достигнуто обеспечением контакта действующего вещества разработанного биотехнологического средства Cellgel с подготовленными патентованным способом клетками кожи, представляющими собой разделенную жизнеспособную гетерогенную популяцию клеток в виде суспензии, для избирательной активации in vitro. Активатор репаративных потенций – это первый практический шаг по направлению строгого различения свойств разнообразных фенотипов субпопуляций клеток кожи и целенаправленного регулирования этих свойств (активация, подавление, видоизменение), с учетом индивидуальных особенностей пациентов с заболеваниями кожи.