Мутации в гене DES человека вызывают тяжелые миопатии и кардиомиопатии [1, 2]. Манифестация заболевания сильно варьирует и может быть с первого и до восьмого десятилетия жизни, причем сведения о доклинических стадиях заболевания крайне малочисленны. Ранние изменения в заболевании являются важной основой для будущих исследований, посвященных влиянию физических упражнений, а также фармакологических вмешательств.
Большинство наследственных миопатий клинически характеризуются прогрессирующей мышечной слабостью [3]. Постоянное нарушение цитоархитектуры скелетных мышц на уровне одного волокна может предшествовать и быть ответственным за прогрессирующую мышечную слабость.
При первично-мышечных заболеваниях морфологические исследования часто обнаруживают следующие изменения мышечных волокон, происходящие в случайном порядке: разнокалиберность размеров с развитием глубокой атрофии отдельных волокон или групп из нескольких близлежащих мышечных волокон, значимая гипертрофия отдельных волокон, продольное расщепление мышечных волокон, базофильные (регенерирующие) мышечные волокна [4].
Диагностика нервно-мышечных заболеваний представляет собой значительную сложность из-за выраженной клинико-генетической гетерогенности [5]. Одним из современных методов диагностики является МРТ мышц, позволяющий предположить, а впоследствии и подтвердить на генетическом уровне диагноз нервно-мышечного заболевания.
Цель исследования - изучение динамики клинической картины миофибриллярной миопатии с мутацией в гене DES c.1021A>C (Thr341Pro) в гетерозиготном состоянии и анализ родословной семьи.
Клиническое описание
Выявленная редкая форма миофибриллярной десмин-зависимой миопатии подтолкнула нас на исследование семьи пациента по линии отца (рис. 1) и подробного анализа течения заболевания у родственников.
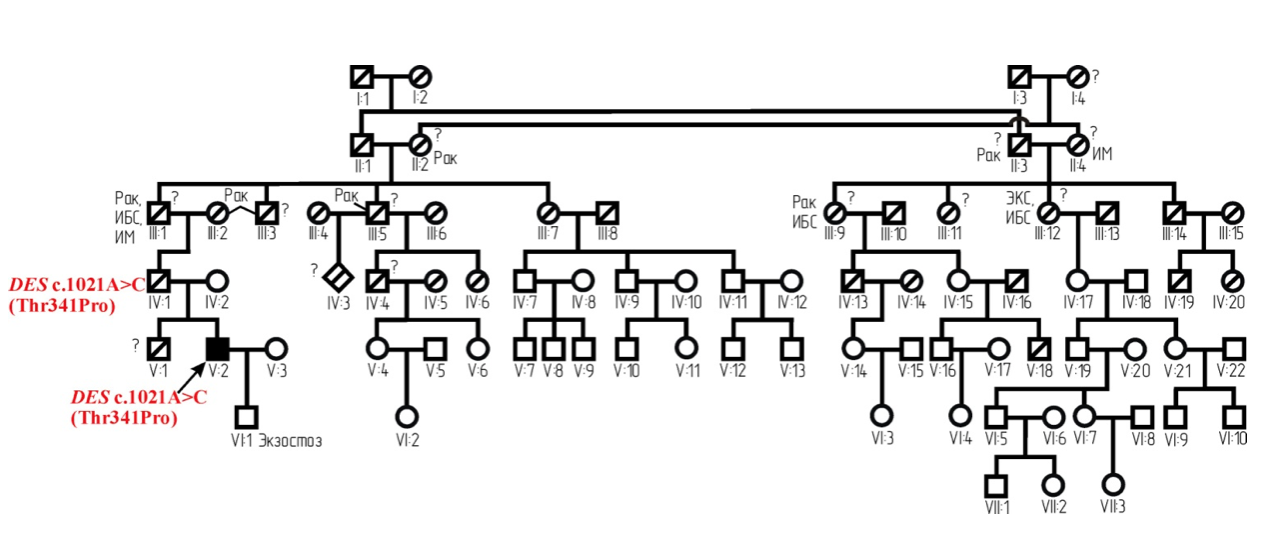
Рис. 1. Родословная семьи с наследственной миофибриллярной десмин-зависимой миопатией: закрашенная фигура V:2 со стрелкой - больной пробанд; IV:1 - больной отец пробанда; перечеркнутые - умершие; римские цифры - поколение; «?» - вероятно больные члены родословной; ИБС - ишемическая болезнь сердца; ИМ - инфаркт миокарда; ЭКС - электрокардиостимулятор; мутации в гене DES выделены красным цветом
Пробанд V:2 родился от второй беременности, первый ребенок (мальчик V:1) умер внутриутробно на 7 месяце беременности. Пробанд рос и развивался по возрасту, активно занимался спортом. В 30-летнем возрасте заметил спотыкания, слабость и усталость мышц, преимущественно нижних конечностей, трудность при подъеме по лестнице, нарушения сердечного ритма. Динамика результатов суточного мониторирования ЭКГ представлена в табл. 1. Неврологический статус пробанда в 33 года: тонус с рук не изменен, с ног снижен, сила в руках 5 баллов, в стопах обоих ног 5 баллов, в проксимальных отделах 3-4 балла, походка «утиная».
Таблица 1. Динамика результатов суточного мониторирования ЭКГ пробанда с десминопатией

Эхокардиография (ЭХО-КГ) пробанда в 34 года: размеры полостей, толщина миокарда, работа клапанов не изменены; добавочная хорда в полости левого желудочка (ЛЖ), сократительная функция ЛЖ удовлетворительная.
В возрасте 35 лет пробанду по МРТ нижних конечностей был предположен клинический диагноз: миофибриллярная миопатия (десминопатия или αβ-кристаллинопатия). Затем методом прямого автоматического секвенирования проведено исследование образца ДНК пробанда и обнаружена замена c.1021A>C (Thr341Pro) в гене DES в гетерозиготном состоянии, мутаций в гене CRYAB не обнаружено. Далее проведена ДНК диагностика отца IV:1 пробанда и обнаружена аналогичная мутация; у сына VI:1 и матери IV:2 пробанда не обнаружена.
Неврологический статус пробанда в 38 лет: мышечная сила в верхних конечностях в левой кисти 4 балла, в правой 3 балла; в проксимальных отделах ног: сгибателях 1 балл, разгибателях 3 балла; мышечный тонус диффузно снижен, гипотрофия мышц плечевого пояса, грудной клетки, передней брюшной стенки, бедер; глубокие рефлексы с верхних конечностей живые симметричные, с нижних конечностей - коленные снижены, аххиловы отсутствуют; нарушений чувствительности нет; передвигается медленно с помощью трости, III группа инвалидности.
Отец IV:1 пробанда по окончании школы прошел двухлетнюю воинскую службу, требуемые физические нормативы успешно выполнял. Жалобы на слабость в ногах появились в возрасте 29 лет. Тогда при обследовании было установлено, что тонус мышц высокий, коленные рефлексы высокие, ахилловы отсутствуют, чувствительных расстройств нет, не может встать на носки и пятки, при ходьбе покачивается, курит с 18 лет. Предположен диагноз инфекционно-аллергический полирадиокулоневрит с нижним вялым парапарезом (стоп). В 30 лет слабость в ногах выросла, тонус снизился, атрофий не было, рефлексы снижены, основные функции сердца не нарушены. Через два года появилась гипостезия стоп и голеней с обеих сторон, причем стопы уже начали свисать. Данные биопсии мышц отца и пробанда представлены в табл. 2.
Таблица 2. Результаты гистологических исследований мышечной ткани семьи с мутацией c.1021A>C (Thr341Pro) в гене DES

На фоне лечения отца пробанда отмечалось ухудшение состояния. Неврологический статус в 33 года: походка паретичная с высоким подъемом ноги так чтобы отвисающая стопа не цеплялась за опору, коленные рефлексы резко снижены, тонус в ногах снижен, брюшные реакции живые, лестничное вставание, сила в руках снижена до 3 баллов, больше слева, в ногах до 2 баллов, гипотрофия мышц обеих голеней, сухожильные рефлексы с рук снижены, гипостезия левой половины лица, на ногах по типу «чулок», на руках по типу «перчаток», передвигается с тростью, II группа инвалидности. В 34 года ошибочно выставлен диагноз спинальная мышечная атрофия. Динамика результатов игольчатой электромиографии (иЭМГ) членов семьи представлена в табл. 3.
Таблица 3. Динамика результатов игольчатой электромиографии членов семьи с мутацией c.1021A>C (Thr341Pro) в гене DES
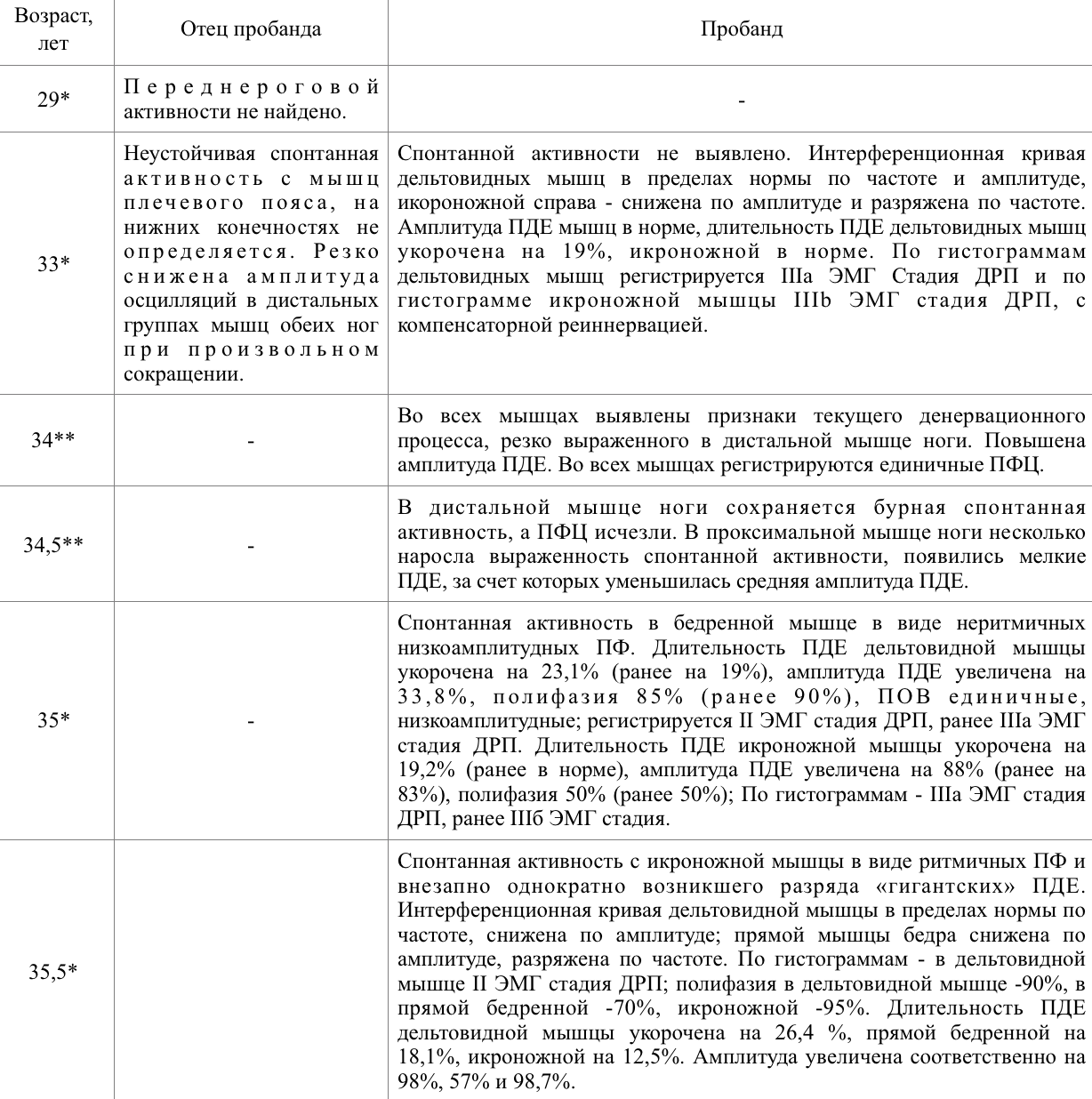
* - исследования выполнены в динамике врачом №1;
** - исследования выполнены в динамике врачом №2.
ПДЕ - потенциал двигательных единиц, ДРП - денервационно-реиннервационный процесс, ПФЦ - потенциалы фасцикуляций, ПФ - потенциалы фибрилляций, ПОВ - положительные острые волны.
С 41 года отец пробанда передвигался в инвалидном кресле, I группа инвалидности. Отмечалась выраженная гипотрофия дистальных отделов верхних и нижних конечностей, выраженный парез кистей – 1 балл, плегия стоп, нарушение функции тазовых органов по типу учащенного мочеиспускания. В следующем году перенес респираторный дистресс-синдром. Смерть отца пробанда наступила от легочно-сердечной недостаточности (пневмонии) в возрасте 49 лет через 20 лет после манифестации заболевания.
Дедушку III:1 пробанда с 35 лет периодически беспокоили боли в эпигастрии (хронический гастрит с пониженной секрецией). В 48 лет острый катаральный аппендицит, удален. В возрасте 46 лет перенес двухстороннюю пневмонию, в 61 и 62 года левостороннюю пневмониию. В 58 лет поставлен диагноз ишемическая болезнь сердца (ИБС). Динамика изменения частоты сердечных сокращений (ЧСС) членов семьи с десминопатией представлена на рис. 2. В 68 лет появилась одышка, уменьшающаяся в положении лежа, установлены стенокардия покоя и напряжения II функционального класса (ФК), признаки хронической коронарной недостаточности боковой стенки, атерокардиосклероз, IIА стадия недостаточности кровообращения.
В 69 лет у дедушки пробанда ночью произошел первый мелкоочаговый рецидивирующий передне-верхушечно-боковой с захватом перегородки инфаркт миокарда. В 70 лет второй инфаркт миокарда с последующей прогрессирующей стенокардией, постинфарктный кардиосклероз. В этом же возрасте обнаружена аденокарцинома прямой кишки II стадии (первые проявления в 67 лет). Проведен 1 этап внутриполостной гамма терапии на опухоль. Последующая ЭКГ сердца зарегистрировала синусовую тахикардию 95 ударов в минуту и обменные нарушения в миокарде. 2 этап прекратили после повторного приступа стенокардии с нарушением обменных процессов, гипоксией миокарда ЛЖ, признаками гипертрофии ЛЖ, диффузными дистрофическими изменениями. Дедушка пробанда умер в возрасте 72 лет от аденокарциномы прямой кишки.
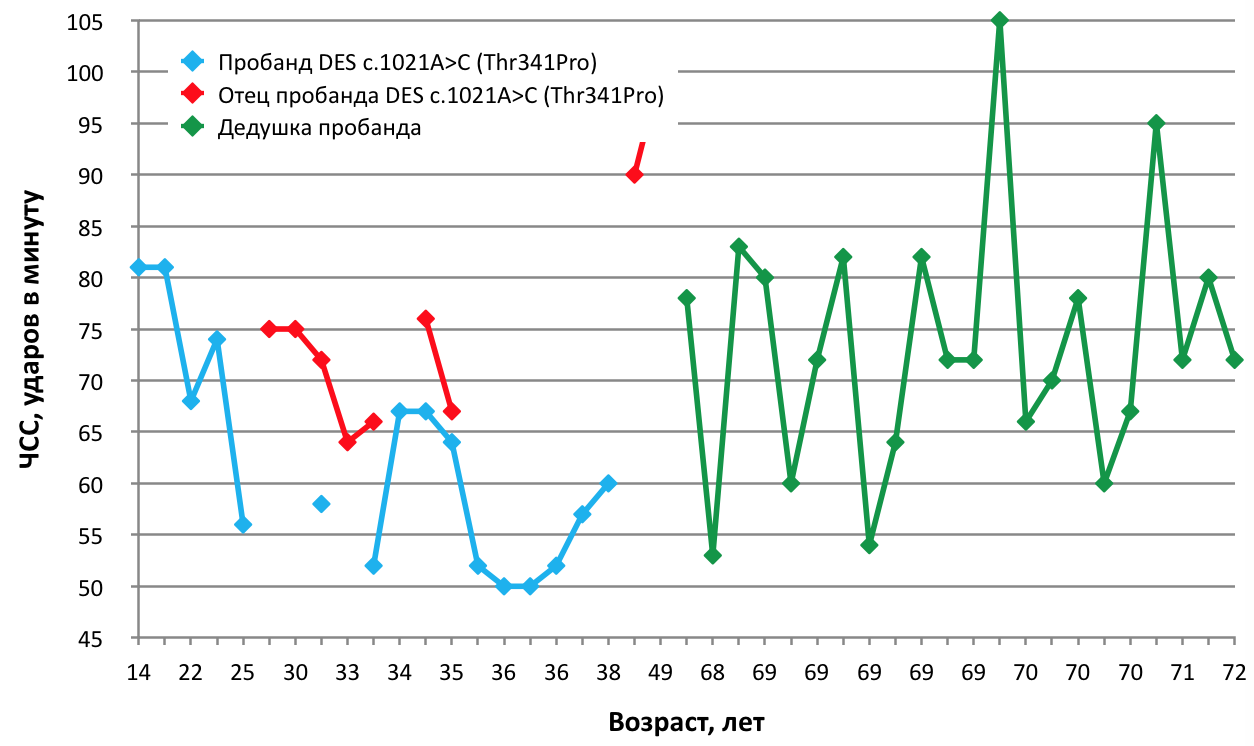
Рисунок 2. Динамика изменения частоты сердечных сокращений (ЧСС) членов семьи с десминопатией
Бабушка III:2 пробанда умерла в возрасте 88 лет от рака лимфоузлов. Старший родной брат III:3 дедушки пробанда умер в возрасте 66 лет от рака предстательной железы. У среднего родного брата III:4 дедушки пробанда был рак мочевого пузыря – скончался в 65 лет. Первый его ребенок IV:3 родился мертвым, второй сын IV:4 умер в 73 года в результате остановки сердца во сне. Родственники IV:6, IV:13, IV:20, V:18 умерли в результате несчастных случаев.
У старшей двоюродной сестры III:9 дедушки пробанда была ИБС, страдала одышкой, умерла в возрасте 78 лет от рака матки. Средняя двоюродная сестра III:11 дедушки пробанда умерла в возрасте 4 месяцев.
У младшей двоюродной сестры III:12 дедушки пробанда в связи с брадикардией, одышкой и АВ-блокадой III степени в 68 лет установлен электрокардиостимулятор (ЭКС). Однако ДНК диагностика не обнаружила у неё замены c.1021A>C (Thr341Pro) в гене DES, но возможно имелись другие мутации десмина. В 88 лет у неё была ИБС, стенокардия напряжения III ФК. ЭХО-КГ показала признаки атеросклероза аорты, кардиосклероза; незначительное снижение сократительной функции миокарда в покое (фракция выброса ЛЖ – 52%); дилатация левых отделов сердца и полости правого предсердия; недостаточность аортального клапана II степени, недостаточность трикуспидального клапана, лёгочная гипертензия. Скончалась в возрасте 88 лет от сердечной недостаточности.
Тетя II:4 дедушки пробанда умерла в возрасте 66 лет от инфаркта миокарда. Дядя II:3 дедушки пробанда скончался от рака мочевого пузыря в 74 года. Двоюродная бабушка I:4 дедушки пробанда умерла в результате сердечной недостаточности. У мамы II:2 дедушки пробанда в 80 лет был выявлен рак кожи - удалена опухоль, скончалась в возрасте 89 лет.
У сына VI:1 пробанда выявлен экзостоз, но результаты ДНК анализа не обнаружили мутации в генах EXT1, EXT2, причем данное заболевание отсутствует как у родственников пробанда, так и у родственников его супруги.

















